Клинические рекомендации по применению богатой тромбоцитами плазмы
Клинический протокол проведения PRP-терапии
На сегодняшний день для лечения дегенеративно-дистрофических и посттравматических заболеваний опорно-двигательного аппарата применяется широкий спектр терапевтических процедур. Наиболее современными из них являются методики регенеративной медицины. Самой распространенной и наиболее изученной является PRP-терапия. PRP (множество тромбоцитов, сконцентрированных в небольшом объеме плазмы крови) — это плазма крови, концентрация тромбоцитов в которой превышает норму [1]. В норме концентрация тромбоцитов колеблется в пределах 180–350 тыс. кл/мкл и в среднем составляет 200 тыс. кл/мкл. Терапевтически эффективной концентрацией препарата PRP считается (хотя количество и подсчет тромбоцитов еще не оптимизированы) концентрация тромбоцитов более 1 млн кл/мкл, т.е. примерно от 4 до 7 раз превышающая средний уровень тромбоцитов в крови [1, 2].

Тромбоциты служат богатым источником факторов роста, цито-хемокинов, а также плазматических белков крови (фибрина, фибронектина, витронектина и др.), которые депонируются в органеллах этих клеток — α-гранулах, электронно-плотных тельцах и лизосомах [1, 2]. Такой коктейль из факторов роста (табл. 1) играет ключевую роль в регуляции процесса восстановления и регенерации тканей, в то время как плазматические белки крови служат в качестве каркаса при регенерации соединительной ткани и миграции эпителиальных клеток [2, 3]. Основные факторы роста накапливаются в α-гранулах, откуда посредством экзоцитоза высвобождаются после активации тромбоцитов во внеклеточную среду. За первые 10 мин тромбоциты секретируют около 70% факторы роста, и далее, в течение 1 ч, происходит практически полное их высвобождение. Синтез дополнительного количества ФР тромбоцитами продолжается еще на протяжении не менее 7 дн, после чего они завершают свой жизненный цикл [4].
В настоящее время описано более 30 факторов роста, содержащихся в α-гранулах тромбоцитов, среди которых особый интерес, в частности для регенеративной медициы, представляют фактор роста эндотелия сосудов (VEGF), тромбоцитарный фактор роста (PDGF), эпидермальный фактор роста (EGF), основной фактор роста фибробластов (β-FGF), трансформирующий фактор роста-β1 (TGF-β1), инсулиноподобный фактор роста (IGF (таблица 1).
Таблица 1. Факторы роста, содержащиеся в микрогранулах тромбоцитов
|
Факторы роста |
Функции |
|
PDGF |
Активация миграции и пролиферации ММСК, фибробластов, гладкомышечных клеток, остеобластов; активация миграции моноцитов, макрофагов, нейтрофилов; активация макрофагов |
|
TGF-β1 |
Индукция синтеза МКМ, регуляция пролиферации кератиноцитов и стимуляция продукции коллагена |
|
VEGF |
Стимуляция пролиферации эндотелиальных клеток и ангиогенеза, стимуляция лимфоангиогенеза, повышение проницаемости сосудистой стенки |
|
EGF |
Стимуляция миграции кератиноцитов, стимуляция пролиферации эпителиальных, мезенхимных клеток и фибробластов; стимуляция миграции и пролиферации эндотелиальных клеток и ангиогенеза, регуляция продукции коллагеназ |
|
FGF |
Индукция пролиферации фибробластов; стимуляция роста эндотелиальных клеток; стимуляция ангиогенеза, стимуляция роста сосудов |
|
IGF |
Стимуляция пролиферации фибробластов, синтез коллагена и других компонентов МКМ |
Согласно последней международной классификации, предложенной объединенным коллективом специалистов из Швейцарии, США, Италии, Польши, Швеции, Голландии, Южной Кореи [5], все препараты PRP подразделяют на 4 категории в зависимости от содержания в них лейкоцитов и фибрина:
- чистая обогащенная тромбоцитами плазма крови
(P-PRP — Pure Platelet-Rich Plasma).
- обогащенная лейкоцитами и тромбоцитами плазма крови
(L-PRP—Leucocyte and Platelet-Rich Plasma)
- чистый обогащенный тромбоцитами фибрин
(P-PRF — Pure Platelet-Rich Fibrin)
- обогащенный лейкоцитами и тромбоцитами фибрин
(L-PRF — Leucocyte and Platelet-Rich Fibrin)
На отечественном рынке предлагается ряд сертифицированных технологий получения PRP и проведения процедуры PRP-терапии (в виде набора необходимых инструментов, емкостей и реактивов), но только некоторые из них сертифицированы. К таковым относятся:
1) REGEN LAB (Швейцария) — РУ № ФСЗ 2011/11417 от 30.12.2011; РУ № ФСЗ 2011/10571 от 30.12.2011;
2) ENDORET-PRGF (Испания) — РУ № РЗН 2014/1995 от 7.11. 2014;
3) YCELLBIO-KIT (Южная Корея) — РУ № РЗН 2014/2149 от 08.12.2014.
Каждая из представленных сертифицированных систем отличается технологическими особенностями приготовления конечного продукта и его составом. Характеристики каждой системы представлены в таблице 2.
Таблица 2. Характеристика основных методов получения PRP-препаратов [6]
|
Класс КПТ |
Продолжительность центрифугирования |
Кол-во тромбоцитов |
Кол-во лейкоцитов |
Объем забираемой крови |
Объем конечного продукта |
Повышение концентрации тромбоцитов (раз) |
|
P-PRP |
Endoret [61] |
невысокое |
нет |
10,0 мл |
5,0 |
2 |
|
L-PRP |
Regen PRP [21] |
высокое |
нет |
8,0 мл |
4,0 |
2 |
|
L-PRP |
YCELLBIOKIT [22] |
Очень высокое |
нет |
15,0 мл |
2,0 |
6-7 |
Наиболее широкое применения в травматологии и ортопедии и спортивной медицине получило применение обогащенная лейкоцитами и тромбоцитами плазма крови (L-PRP— Leucocyte and Platelet-Rich Plasma). Основываясь на мировом опыте применения данных коммерческих систем, для выделения PRP и характеристиках получаемого продукта, для использования нами была выбрана система YCELLBIOKIT, как наиболее эффективная. Данная система позволяет получить наибольшее количество тромбоцитов с максимальной концентрацией в полученной плазме. Это позволяет достичь максимально-выраженного и продолжительного терапевтического эффекта при лечении как дегенеративно-дистрофических, так посттравматических заболеваний опорно-двигательного аппарата.
Протокол получения L-PRP
L-PRP выделяют при помощи сертифицированной системы YCELLBIOKIT (зарегистрированное медицинское изделие № РЗН 2014/2149 от 08.12.2014) на центрифуге Армед 80-2 (зарегистрированное медицинское изделие № ФСЗ 2012 / 12304 от 07.06.2012) с использованием антикоагулянта ACD-A (Раствор соответствует ФСП-42-0566-5847-04. Контейнеры с раствором отвечают требованиям ТУ 9393-004-99119410-2010 Производитель Резерв-М, Росиия).
Проведение процедуры выделение L-PRP и последующее введение в зону патологического процесса происходит в асептических условиях перевязочной отделения травматологии и ортопедии.
Для проведения данной процедуры требуется
- Контейнер YCELLBIO (1 шт.);
- Кровь (15 мл);
- Антикоагулянт (1,5 мл);
- Шприц на 20 см3 (1 шт.);
- Шприц на 5 см3 (1 шт.);
- Шприц на 2 см3 (1 шт.);
- Игла калибра 21G или игла «бабочка» (1 шт.);
- Игла калибра 18G с длиной 40 мм (2 шт.);
- Вата, смоченная в спирте / Пинцет.
Порядок получения крови и выделения L-PRP
- Заберите шприцом 1,5 мл антикоагулянта (Перед забором крови важно, чтобы внутренняя поверхность цилиндра шприца была обработана антикоагулянтом) Нами используется рекомендованный производителем антикоагулянт ACD-A (раствор цитратного гемоконсерванта с декстрозой);
- Заберите 13,5 мл крови в шприц с антикоагулянтом, чтобы в конечном итоге получилось 15мл раствора. (13.5мл крови+1.5мл антикоагулянта).
- Используя иглу 18G, влейте собранную кровь в контейнер YCELLBIO (под углом 45˚) до соответствующей метки.
- Поместите пробирку с кровью в центрифугу (Армед 80-2, угловой ротор) и центрифугируйте со скоростью 3400~3600 об. в мин. с центробежной силой 1900*g ~ 2000*g в течении 6-8 минут. Цель центрифугирования – поместить гематокритный слой ниже горловины пробирки.
- После окончания центрифугирования вынуть пробирку из центрифуги и оценить положение гематокритного слоя в пробирке. В случае его нахождения в горловине пробирки перейти к следующему шагу. В случае его нахождения ниже горловины пробирки, вращая регулирующий колпачок по часовой стрелке поднять гематокритный слой до уровня горловины. В случае нахождения гематокритного слоя выше горловины- повторить процедуру центрифугирования в прежнем режиме в течении 2минут.
- Приготовьте 3 см3 шприц с иглой 18G для извлечения слоя PRP; Заберите 1,5 – 2 мл PRP из горловины. Слегка взболтайте плазму иглой, чтобы осевшие тромбоциты поднялись.
- После 3-х кратной обработки области введения L-PRP, произвести введение полученного раствора в пораженную область.
- По завершении процедуры введения наложить асептическую повязку на область пункции.
Перечень показаний для проведения PRP-терапии.
При лечении дегенеративно-дистрофических заболеваний опорно-двигательного аппарата (деформирующий остеоартроз 1-3 степени плечевого, локтевого, лучезапястного, тазобедренного, коленного и голеностопного суставов) применяется 3-х кратное введение L-PRP в поврежденный сустав с интервалом введения 5-7 дней. Возможно комбинирование с препаратами гиалуроновой кислоты [7-13].
Для лечения хронических заболеваний опорно-двигательного аппарата воспалительной природы (энтезопатии связочного аппарата, эпикондилиты, эпифасцииты, тендиниты, лигаментиты, бурситы, тендинопатии) применяется от 1 до 3 инъекций L-PRP в пораженную структуру, в зависимости от степени выраженности процесса и объеме тканей, вовлеченных в патологический процесс с интервалом 5-7 дней. [14-17]
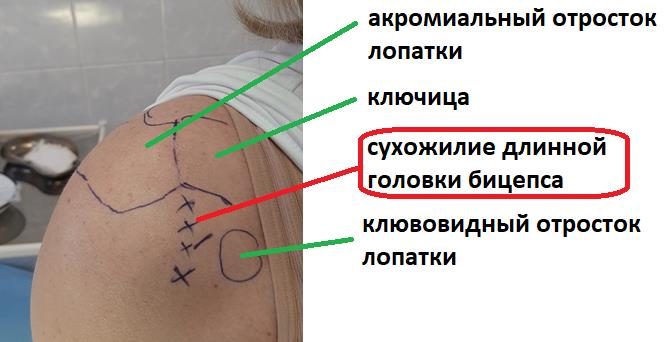
При лечении острых повреждений мягких тканей проводится 1-2 курса PRP-терапии в поврежденные мягкие ткани на 5-10 сутки с момента травмы, после начала организации посттравматической гематомы.
Возможно применение PRP-терапии в сочетании с оперативными техниками как в раннем, так и позднем послеоперационном периоде (шов сухожилий, восстановление после разрыва ПКС, состояния после менискэктомии и микрофрактурации). Проводится курс 3 инъекций L-PRP в оперированную область с интервалом 5-7 дней. [18-20]
Противопоказания для проведения PRP-терапии.
|
|
|
|
|
Перечень обследований необходимых для проведения PRP-терапии.
При лечении дегенеративно-дистрофических заболеваний опорно-двигательного аппарата необходимо:
- Рентгенография пораженного сустава
- МРТ пораженного сустава
- Общий анализ крови
При лечении хронических заболеваний опорно-двигательного аппарата воспалительной природы необходимо:
- УЗИ мягких тканей области воспалительного процесса
- Общий анализ крови
При лечении острых повреждений мягких тканей необходимо:
- УЗИ мягких тканей в области повреждения
- В некоторых случаях МРТ области травмы
- Общий анализ крови
Список Литературы
- Marx R. Platelet rich plasma (PRP): What is PRP and what is not PRP? Implant dent 2001; 10: 225.
- Arshdeep, Kumaran М. Platelet-rich plasma in dermatology: Boon or a bane? Ind J Dermatol Venereol Leprol 2014; 80: 5–14.
- Sommeling C., Heyneman A., Hoeksema H., Verbelen J., et al. The use of platelet-rich plasma in plastic surgery: A systematic review. J Plast Reconstr Aesthet Surg 2013; 66: 301–312.
- Marx R. Platelet-rich plasma: evidence to support its use. J Oral Maxillofac Surg 2004; 62: 489–496.
- Ehrenfest D.M., Bielecki T., Mishra A., et.al. In search of a consensus terminology in the field of platelet concentrates for surgical use: plateletrich plasma (PRP), platelet-rich fibrin (PRF), fibrin gel polymerization and leukocytes. Curr Pharm Biotechnol 2012; 13 (7): 1131–1137.
- Ehrenfest D., Rasmusson L., Albrektsson T. Classification of platelet concentrates: from pure platelet-rich plasma (P-PRP) to leucocyte- and platelet-rich fibrin (L-PRF). Trends Biotechnol 2009; 27 (3): 158–167.
- Gobbi A, Lad D, Karnatzikos G. The effects of repeated intra-articular PRP injections on clinical outcomes of early osteoarthritis of the knee. Knee Surg Sports Traumatol Arthrosc 2015;23:2170-7.
- Kreuz PC, Kruger JP, Metzlaff S, et al. Platelet-Rich Plasma Preparation Types Show Impact on Chondrogenic Differentiation, Migration, and Proliferation of Human Subchondral Mesenchymal Progenitor Cells. Arthroscopy 2015.
- Gobbi A, Karnatzikos G, Lad D. Knee Cartilage Lesions Management in Professional Athletes. Sphera Medical Journal 2014;10:30-8.
- Gobbi A, Lad D, Karnatzikos G. International experience with cartilage repair. In: ISMF 2014 Carlsbad, California; 2014.
- Mangone G, Orioli A, Pinna A, Pasquetti P. Infiltrative treatment with Platelet Rich Plasma (PRP) in gonarthrosis. Clinical cases in mineral and bone metabolism : the official journal of the Italian Society of Osteoporosis, Mineral Metabolism, and Skeletal Diseases 2014;11:67-72.
- Renevier JL, Marc JF. Etude Pilote d'un dispositif médical intra-articulaire innovant dans la prise en charge de la gonarthrose symptomatique fémoro-tibiale grade II-III radiologique après échec d'un AH. Revue du Rhumatisme 2014;81:A202.
- Napolitano M, Matera S, Bossio M, et al. Autologous platelet gel for tissue regeneration in degenerative disorders of the knee. Blood Transfus 2012;10:72-7
- Papalia R, Franceschi F, Carni S, et al. Intra-Articular injections for degenerative cartilage lesions of the knee: platelet rich plasma vs hyaluronic acid. Muscles, ligaments and tendons journal 2012;2 (3 — Suppl)
- Crescibene A, Napolitano M, Sbano R, Costabile E, Almolla H. Infiltration of Autologous Growth Factors in Chronic Tendinopathies. Journal of blood transfusion 2015;2015:924380.
- Giannotti S, Dell'Osso G, Bottai V, et al. Treatment of Tendon Injuries of the Lower Limb with Growth Factors Associated with Autologous Fibrin Scaffold or Collagenous Scaffold. Surg Technol Int 2015;26:324-8.
- Gobbi A, Karnatzikos G, Malchira S, Kumar A. Platelet Rich Plasma (PRP) in Osteoarthritis. In: Lana JFSD, Santana MHA, Belangero WD, Luzo ACM, eds. Platelet-Rich Plasma; Regenerative Medicine: Sports Medicine, Orthopedic, and Recovery of Musculoskeletal Injuries: Springer Berlin Heidelberg; 2014:231-6.
- Gobbi A, Karnatzikos G, Sankineani SR. Role of cell therapies in ACL repair. Sphera Medical Journal 2013;9:22-6
- Gumina S, Campagna V, Ferrazza G, et al. Use of platelet-leukocyte membrane in arthroscopic repair of large rotator cuff tears: a prospective randomized study
- Conz C, Karnatzikos G, Bevilacqua S, Gobbi A. Proteggi, ripara, presto! Sport & Medicina 2010;5:18-23.
- Andia I., Abate M. Platelet-rich plasma: underlying biology and clinical correlates. Regen Med 2013; 8 (5): 645–658.
- Ткачев В., Барунова Н., Халдина М. и др. Технология YCELLBIO-KIT для приготовления L-PRP — аутологичной плазмы, обогащенной тромбоцитами и лейкоцитами // Новая косметология. Трихология: диагностика, лечение и уход за волосами. М.: ИД ≪Косметика & Медицина≫, 2015.